双抗license out大爆发背后:两个风口与潜力新星
来源:医药魔方 2024-12-10 09:09
国内药企在双抗药物研发领域,技术平台日益成熟,靶点组合探索能力也不断深化。
2024年,国产双抗药物热度飙升,交易呈现大爆发态势,无论交易数量还是合作规模,都远超以往。这不仅体现了国产Biotech在双抗领域的研发实力,也反映了全球市场对于中国创新药物的认可和需求。

近5年双抗交易趋势分析
尤其2024下半年的双抗药物交易尤为火热,共发生14笔对外授权交易。其中,有两类交易备受瞩目。一类是PD-1/VEGF双抗,这主要基于依沃西单抗在与K药的头对头研究中,显示了疗效优势,代表着PD-(L)1药物升级迭代的新方向,同时也凸显了肿瘤治疗领域对于创新疗法的迫切需求。另一类则是T细胞衔接器(TCE),这主要得益于其在自身免疫性疾病中展现出的巨大应用潜力。
2024下半年国产双抗相关交易
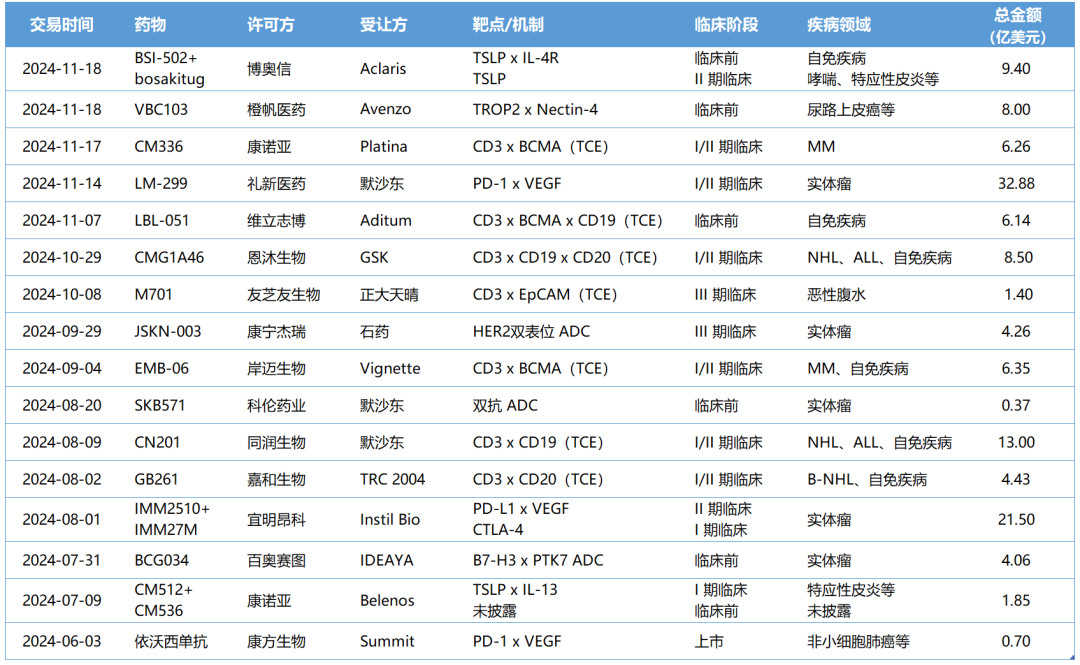
注:数据来源于医药魔方数据库,包含两笔三抗TCE交易;依沃西单抗2022年已以总金额50亿美元授权给了Summit,表格中交易为扩大许可地区
PD-1/VEGF双抗疗效成功验证,掀起同类药物交易热潮
今年9月,世界肺癌大会(WCLC)上公布的III期HARMONi-2研究结果显示,依沃西单抗在头对头比较中优于K药,这无疑点燃了业界对于PD-1/VEGF双抗的热情。
距全球首款PD-1单抗问世至今已有10年,目前已有20余种PD-(L)1药物上市,在这个潜力巨大又充满迭代竞争的市场中,各方都在竭力寻找新的突破点,以期在未来市场占据更有利的位置。疗效结果通常是衡量药物临床价值的关键指标,经HARMONi-2研究验证有效的依沃西单抗显然具有很强的借鉴意义。后续,宜明昂科的PD-L1/VEGF双抗IMM2510以21亿美元授权给Instil,礼新医药的PD-L1/VEGF双抗LM-299以32亿美元授权给默沙东,交易金额在今年所有的License-out交易中也是位居前列。
依沃西单抗的部分海外开发和商业化权益早在两年前就被康方生物以50亿美元授权给了英国公司Summit,彼时,这一金额刷新了中国生物医药企业License-out交易的纪录。今年6月,两家公司又修订了许可协议,进一步扩大了Summit在海外的许可地区。随着这次PD-1/VEGF双抗的爆火出圈,再加上之前康方生物另一款PD-1/CTLA-4双抗也已获得成药验证,一场关于PD-1双抗的大戏缓缓拉开帷幕,代表着PD-1抑制剂升级迭代一个较为确定的新方向。
在这一全新战场中,众多国产Biotech们已然提前布局,蓄势待发。普米斯是拥有PD-(L)1双抗药物最多的企业之一。该公司自主研发的PD-L1/VEGF双抗PM8002已步入III期临床阶段,进度领先或许是BioNTech9.5亿美元收购普米斯的最主要原因。除了PM8002,普米斯还拥有其他5款PD-(L)1双抗,靶点分别涵盖TIGIT、TGF-β、4-1BB、CD40。此外,普米斯还拥有EGFR/cMET、4-1BB/CLDN18.2、TIGIT/PVRIG、CCR8/CTLA-4这四款双抗。
PD-(L)1双抗赛道中,恒瑞的PD-L1/TGF-βRII双功能融合蛋白已经申报上市,在全球范围内都属于进度领先。此外,普米斯(BioNTech)的PD-1/VEGF双抗、默克的PD-L1/TGF-β双抗、康宁杰瑞的PD-L1/CTLA4双抗、阿斯利康的PD1/CTLA4双抗、Compugen和阿斯利康合作开发的PD-1/TIGIT双抗、Genmab的PD-L1/4-1BB双抗、MacroGenics和再鼎医药合作开发的PD-1/LAG3双抗均已步入III期临床阶段。PD-(L)1双抗能否成功取代现有的PD-1药物,实现全面的迭代升级?让我们共同拭目以待。
突破血液瘤局限,TCE站上自免风口
2024下半年,另一类吸睛的创新药交易当属TCE。短短4个月内,这个赛道便发生了7笔交易,其中5款药物的开发目标指向了自身免疫性疾病适应症。在这些交易中,金额最高的两笔分别是同润生物与默沙东达成的CD3/CD19双抗TCE交易(13亿美元),以及恩沐生物与GSK达成的CD3/CD19/CD20三抗TCE交易(8.5亿美元)。
TCE作为一种可同时结合靶细胞表面的相关抗原和T细胞表面TCR复合物中的CD3的双抗,能够引导和激活T细胞对目标进行精准打击。这类药物对于市场而言并不陌生,目前全球范围内已上市的此类药物已达10余个。随着技术进步,近年来,三抗等不同类型的TCE也逐步被开发。从作用机制上看,TCE与嵌合抗原受体T细胞(CRA-T)极为相似。
已上市的TCE药物
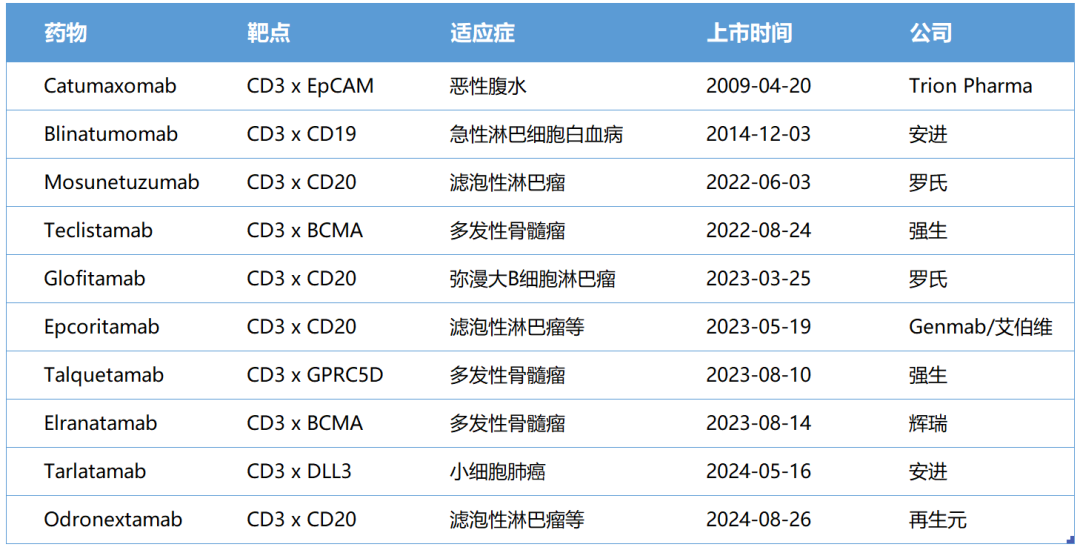
注:Catumaxomab已退市
TCE和CAR-T疗法已经在B细胞病变相关的恶性血液瘤中展示出了显著效果,并且已有多款药物成功上市。然而在实体瘤中,由于大多数靶点(如HER2等)也在正常组织中表达,T细胞攻击目标时容易“误伤”,并且肿瘤微环境(TME)中还存在免疫抑制,这增加了TCE和CAR-T在实体瘤领域的开发难度,目前仅有一款安进靶向CD3/DLL3的TCE被FDA加速批准用于治疗小细胞肺癌。
在自身免疫性疾病领域,近20年来,B细胞耗竭疗法(BDCT)始终是主要的治疗手段之一,例如靶向CD20的利妥昔单抗等。然而,由于B细胞生命周期表面抗原表达的差异化以及疾病的复杂性,现有疗法无法实现对B细胞的完全清除,导致疗效有限。随着TCE和CAR-T疗法在肿瘤领域大获成功,尤其是其展现出的对B细胞的深度清除能力,科学家们开始探索它们在自身免疫性疾病领域的应用。
2021年8月,《新英格兰医学》上发表的一项研究显示,一名患有严重性系统红斑狼疮的患者在接受CD19 CAR-T治疗后,病情得到了缓解。2024年4月,《自然·医学》上发表的一项研究显示,靶向CD3/CD19的TCE贝林妥欧单抗(Blinatumomab)成功治疗了6名患有严重多重耐药的类风湿性关节炎患者。随后,又有证据表明靶向CD3/BCMA的TCE特立妥单抗(Teclistamab)在系统性红斑狼疮患者中有效。越来越多证据显示CAR-T和TCE疗法在自身免疫性疾病领域具有广阔的应用前景。
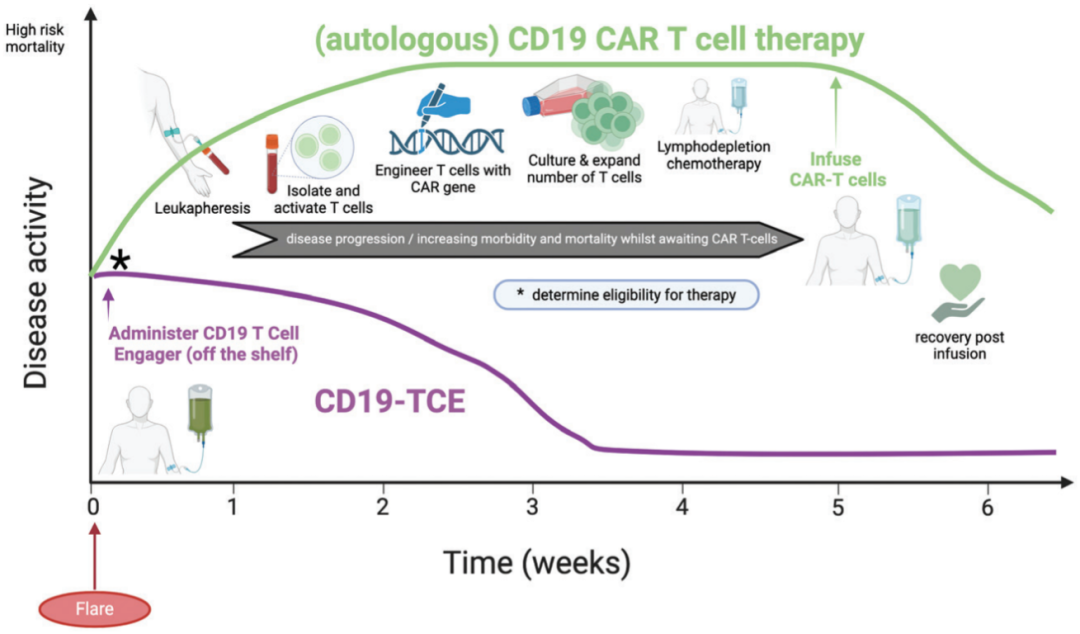
CAR-T与TCE在自身免疫性疾病中应用的对比
来源:Clin Exp Immunol
然而个体化制备的CAR-T疗法生产成本高、周期长、对医疗设施和专业团队的要求很高。相比之下,TCE疗法易于生产,还可能制作成皮下注射剂型,可以更快应用于临床,可及性方面具有优势。正是因为看重了TCE在自身免疫性疾病领域所展现出的巨大潜力,各大药企纷纷积极布局,使其热度不断攀升,成为了行业内备受关注的焦点。
国产双抗还有哪些宝藏资产?
在当前双抗交易火爆的态势下,中国药企当中能否再度出现幸运儿?诚然,这股双抗的“东风”还能持续多久尚不可知,不过我们或许可以从各家biotech的在研管线当中,探寻一下这个黄金赛道的潜力产品。
对于当下最火热的PD-(L)1/VEGF双抗,除了上文中提到的几家公司之外,华博生物、三生国健、天力士/圆祥生命科技、荣昌生物、明慧医药、神州细胞、广州昂科免疫、尚健生物、君实生物、甫康药业等公司都有相关的在研产品已进入临床研究阶段。
已上市及临床阶段的国产PD-(L)1/VEGF双抗
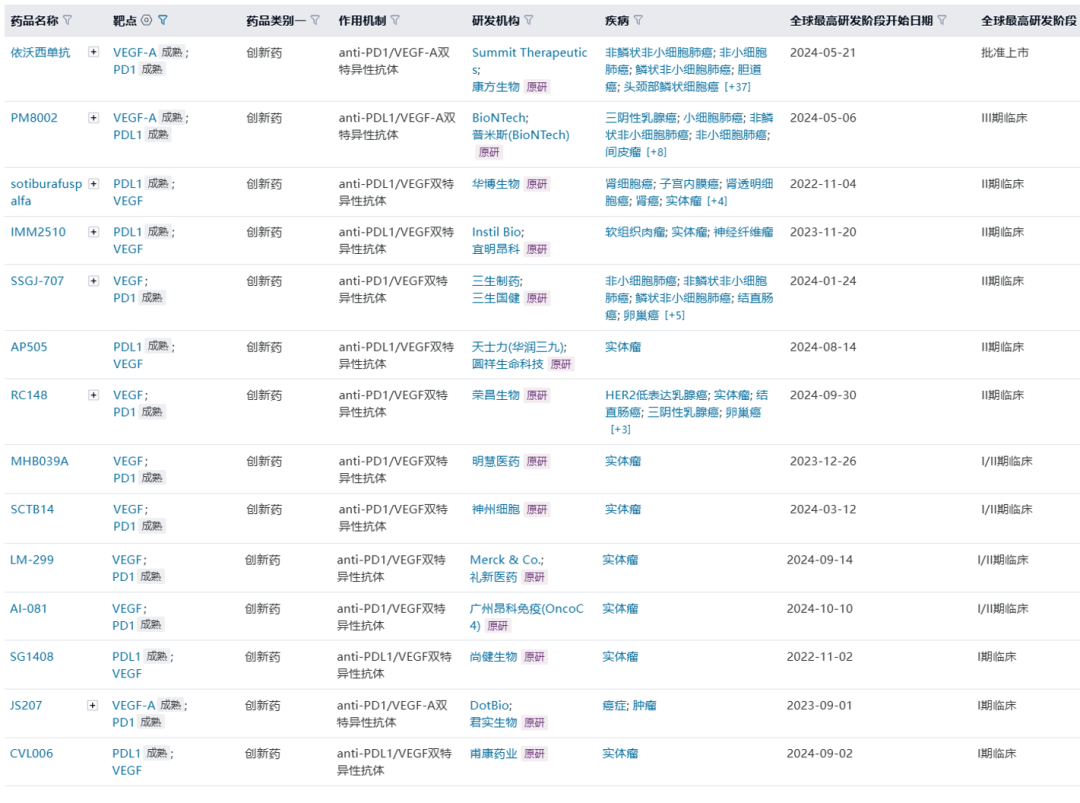
数据来源:医药魔方NextPharma数据库
TCE自免应用领域,靶向CD3/BCMA的双抗中,除上述已达成相关交易的岸迈生物和康诺亚外,智翔金泰、正大天晴、新时代药业、益科斯特也有同类产品进入临床研究阶段;靶向CD3/CD19的双抗中,除同润生物外,益科斯特、亿一生物、绿竹生物、新时代药业的同类产品也已进入临床研究阶段;靶向CD3/CD20的双抗中,爱思迈、康诺亚、亿腾嘉和、天广实、正大天晴、君实生物、神州细胞的同类产品也已进入临床研究阶段。
从公司角度来看,普米斯以其丰富的双抗管线被国际巨头BioNTech收购。康方生物不仅手握两款商业化PD-1双抗产品,管线中还有两款PD-1双抗(分别靶向LAG-3和CD73)处于早期临床研究阶段,一款PD-1/CD73双抗处在临床前研究阶段。此外,康方生物在实体瘤领域的CD47/CLDN18.2双抗已进入I期临床,CD73/LAG-3双抗已申报IND。
部分国产公司双抗管线梳理
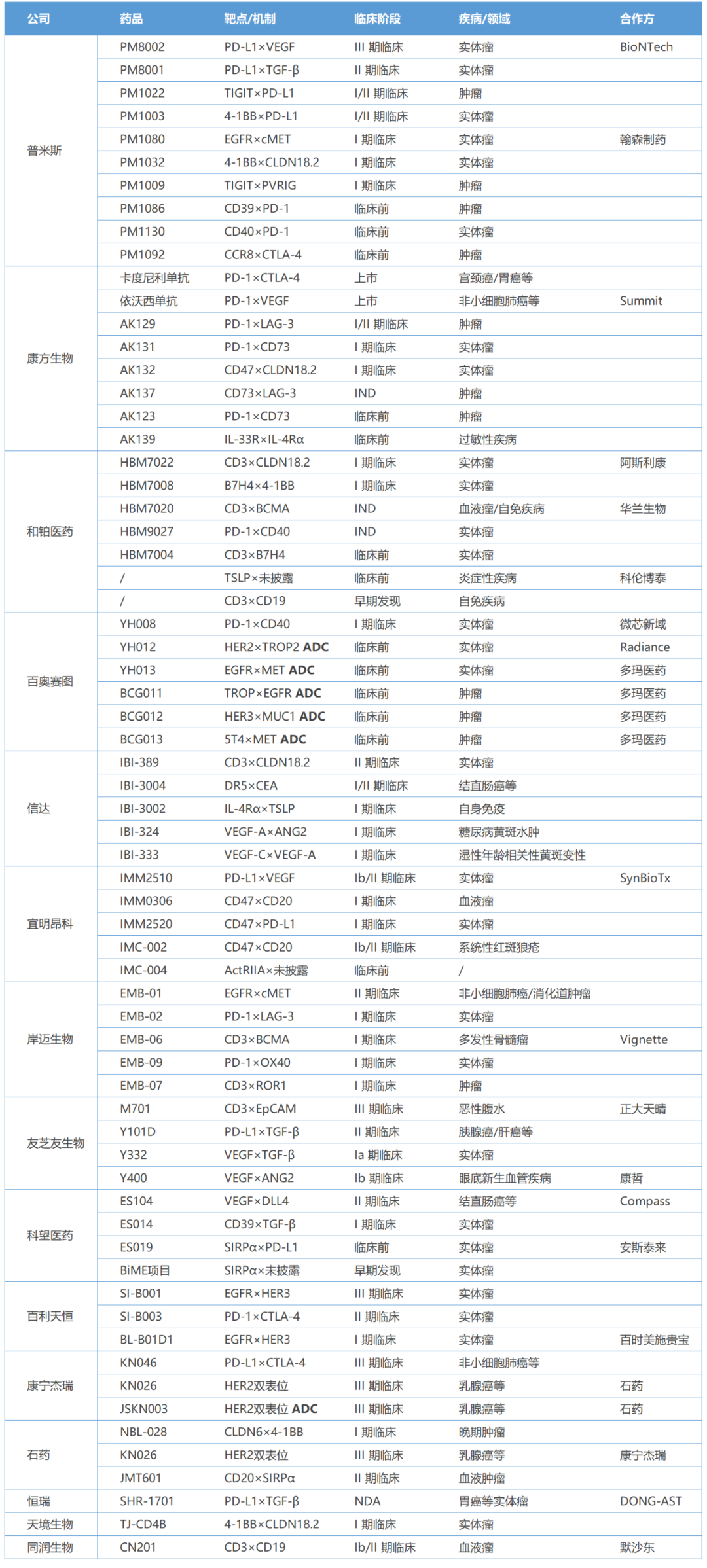
注:整理自各公司官网披露的管线进展
和铂医药也有一款PD-1/CD40双抗处于IND阶段。值得注意的是,这家公司TCE管线较多,其中一款CD3/CLDN18.2双抗已与阿斯利康建立起了合作,另一款CD3/BCMA双抗也和华兰生物合作开发,另还有两款双抗TCE处于临床前研究阶段(CD3/B7H4双抗、CD3/CD19双抗)。
拥有五款双抗的信达生物,在数量方面已然不算少。其中,CD3/CLDN18.2双抗已进入II期临床阶段,研发进度在全球范围内都属领先,另外信达还将双抗的应用拓展至眼科领域,两款VEGF-A双抗均已步入I期临床。百奥赛图的双抗管线主要以双抗ADC药物为主,除此之外,还有一款PD-1/CD40双抗已进入I期临床。
除上述公司外,宜明昂科、岸迈生物、友芝友生物、百利天恒、科望医药、康宁杰瑞等公司的双抗管线中至少有一款PD-1双抗。TCE药物方面,岸迈生物还拥有一款CD3/ROR1双抗。另外,友芝友生物靶向CD3/EpCAM的双抗进展较快,已步入III期临床阶段。
通过对这些国产Biotech的双抗管线梳理可以发现,国产双抗的实力相当强劲。当然,还有许多拥有优质双抗管线的Biotech并未在此一一罗列出来。
总而言之,国内药企在双抗药物研发领域,技术平台日益成熟,靶点组合探索能力也不断深化。与此同时,国产双抗药物不但在国内市场中崭露头角,还在全球市场中积极寻求机遇与挑战。其国际化进程正在加速推进,未来发展充满着无限潜力。
参考资料:
[1]Shah K, Leandro M, Cragg M, et al. Disrupting B and T-cell collaboration in autoimmune disease: T-cell engagers versus CAR T-cell therapy?. Clin Exp Immunol. 2024;217(1):15-30. doi:10.1093/cei/uxae031
[2]Robinson WH, Fiorentino D, Chung L, et al. Cutting-edge approaches to B-cell depletion in autoimmune diseases. Front Immunol. 2024;15:1454747. Published 2024 Oct 9. doi:10.3389/fimmu.2024.1454747
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


